《実験結果》
結果は、グラフ1、2のようになった。
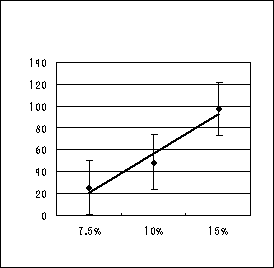
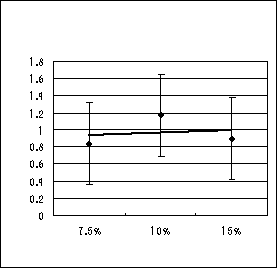
グラフより、
・塩化アンモニウムの濃度を上げると電流値があがるが電圧は変わらない。
その他として、
・時間がたつにつれ電流値は下がり、電圧は上がる。
・炭素棒をかき混ぜると電流値は上がる。
《考察》
グラフ1を見ると、塩化アンモニウム水溶液濃度が上がると電流値が上がっている。これは、濃度が高く
なった事により、NH4+の量が増えるためだと考えられる。この実験において、亜鉛版で生じたZn2+は、
NH4+と反応して錯イオン〔Zn(NH3)4〕2+が生じる。このイオンによって、亜鉛のイオン化が阻害
されないため、このような結果になったと考えられる。
放電時間と電流値・電圧の関係についてであるが、この実験の反応は次の様になっている。
この反応によって生じるZn(NH3)2Cl<>2が電解液中に析出し、電気抵抗が、放電が進むにつれ大き くなるため、電流値が下がったと考えられる。また、放電が進むにつれて、電気抵抗が大きくなり、電流 値が小さくなったために、電圧が上がったものと考えられる。 また、炭素棒をかき混ぜると電流値が上がったことについては、負極と炭素棒が接する面積が大きくな ったために、電流が流れやすくなったから、このようになったと考えられる。